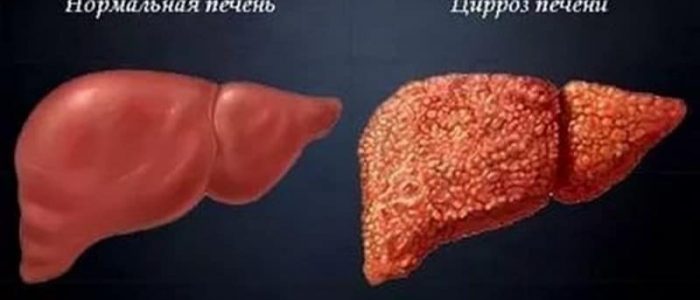
Болезни печени и суставы
Может ли цирроз печени либо другие патологические изменения этого органа влиять на суставы, вопрос, который нередко звучит из уст пациентов в кабинете ревматолога. Спровоцировать болезни суставов способны различные нарушения в человеческом организме, в частности, на состояние костно-мышечной системы влияют неполадки в работе печени. Крупнейшая пищеварительная железа, отвечающая за выработку желчи, призвана обезвреживать токсические вещества, переизбыток которых негативно отражается на многих внутренних органах и системах организма, не оставляя без внимания и подвижные соединения костей скелета.
Взаимосвязь заболеваний печени и суставов
Печень является многофункциональным органом, который принимает участие более чем в 500 различных реакциях. Пищеварительная железа выполняет следующие функции, важные для человеческого организма:
- фильтрует кровь и создает запасы витаминов, гемоглобина, сахара;
- выступает защитой от проникновения ядовитых и вредоносных веществ;
- вырабатывает желчь, которая необходима для расщепления и переваривания жиров, содержащихся в пище;
- ликвидирует большинство гормонов.
Нарушенная деятельность печени опасна загрязнением организма.
Таким образом, сторонники Аюрведы аргументируют связь больных суставов и печени тем, что патологии костно-мышечной системы нередко являются результатом зашлакованности организма. В связи с этим, проблемы с фильтрационным органом и как следствие недостаточный контроль обменных процессов в хрящевой ткани — одна из основных причин возникновения болей в мышцах и суставах, которым предшествует разрушение соединительнотканных структур костных сочленений.
Здоровый орган содержит специфические клетки, которые синтезируют вещество, поступающее по лимфе и кровяной жидкости к суставам. Этот элемент способствует регенерации и восстановлению хрящевой ткани, а также улучшает кровоснабжение костно-мышечного аппарата. Однако если «строительного материала» в крови недостаточно, то ухудшается питание суставов и в результате под воздействием постоянных нагрузок, они начинаются крушиться. Кроме этого, плохая работа печени влияет и на межпозвонковые хрящи, которые начинают разрушаться, а позвонки, смещаясь, зажимают нервные окончания. Итогом этого являются различные заболевания.
Чем грозят проблемы с печенью?
Увеличение печени — опасное патологическое состояние, которое негативно отражается на функциональности многих органов и систем человеческого организма. Нередко на фоне печеночных болезней у больного развивается ревматоидный артрит, при котором сильно болят суставы, отмечается утренняя скованность и затекание тела. Значительно ухудшается общее самочувствие, повышается температура тела, ухудшается аппетит, и пациенты жалуются на постоянную слабость. Кроме ревматоидного артрита, нередко у больных с патологиями печени развивается спондилоартроз. При этом недуге людей беспокоит выраженная боль в позвоночнике, после чего становится трудно передвигаться и совершать движения.
Лечебные мероприятия
Для торможения развития суставных заболеваний, в первую очередь, необходимо предпринять меры, чтобы перестала болеть печень — главная виновница проблем с опорно-двигательным аппаратом. Для этого рекомендуется придерживаться следующих рекомендаций:
- Наладить режим питания, увеличив количество трапез до 5-ти раз в сутки. При этом порции должны быть небольшими, чтобы не перегружать желудок.
- Сократить потребление жирной пищи, заменив животные жиры растительными.
- Заменить сдобу хлебом крупного помола, каши и картофель — овощами, шоколад и прочие сладости — сухофруктами, фруктами.
- Отказаться от ночного приема пищи. Последняя трапеза должна быть за 4 часа до сна.
Кроме этого, важно регулярно принимать медикаментозные препараты, которые улучшают функционирование печени и защищают ее клетки от негативного воздействия окружающих факторов.
Чтобы не допустить развития осложнений суставных патологий, не следует затягивать с лечением. Поэтому вместе с мероприятиями, направленными на улучшение состояния печени нужно приступить и к борьбе с болезнями суставов. Унять боль и снять воспалительный процесс под силу нестероидным противовоспалительным средствам. Вместе с местным лечением отличные результаты показывает физиотерапия.
Профилактика
Предупредить болезни печени и не дать пострадать суставам можно с помощью несложных мероприятий. Всем людям без исключения рекомендуется следить за своим питанием и образом жизни. Еда должна быть не только вкусной, но и полезной, спорт — в меру, без лишних интенсивных нагрузок на костно-мышечный аппарат. Помимо этого, важно следить за здоровьем и своевременно обращаться к врачу.
Источник статьи: http://etosustav.ru/zabolevania/obshee/bolezni-pecheni-i-sustavy.html
Патология печени при ревматоидном артрите Текст научной статьи по специальности « Клиническая медицина»
Похожие книги на litres.ru
Похожие темы научных работ по клинической медицине , автор научной работы — Вратских Е. В., Балабанова Р. М.
Текст научной работы на тему «Патология печени при ревматоидном артрите»
ПАТОЛОГИЯ ПЕЧЕНИ ПРИ РЕВМАТОИДНОМ АРТРИТЕ
Е.В. Братских, P.M. Балабанова ГУ Институт ревматологии РАМН, Москва
Суть патологического процесса при ревматоидном артрите (РА) состоит в генерализованном иммунологическом (аутоиммунном) воспалении, приводящем к развитию си-новита, а также широкого спектра внесуставных органных проявлений [3], из которых патология желудочно-кишечного тракта составляет 11%, включая гепатомегалию в 19,5 % из них [23].
Взгляды на причины и характер печеночной патологии при РА менялись с течением времени в зависимости от точки зрения исследователей на патогенез заболевания, расширения спектра лекарственных, нередко гепатотоксичес-ких, средств, применяемых в ревматологии.
В 60-е годы обсуждалась роль первичного очага воспаления — синовиальной ткани как индуктора аутоаллергических процессов (T.Higashi,F.Hasegava, 1960); органоспецифических аутоантител (Л. Т. Пяй, 1967), повышенной проницаемости сосудистой стенки, нестабильности гепатоци-тов, приводящей к гиперферментемии, диспротеинемии (Р.Вогее!, Е.Рес1еге,1961); уменьшения резерва витаминов, нарушения ферментативной функции (М.Е. Курмае-ва,1969) и кровообращения в печени (В. Ф. Сысоев, Э. С. Мач, 1966) [цит. по 9].
Различалась и трактовка изменений функциональной способности печени. Большинство исследователей уже на ранней стадии РА отмечали нарушение её дезинтоксикаци-онной, пигментной, белковообразующей и углеводной функции, другие считали, что функция органа страдает только при амилоидном поражении (24]. Структурные изменения, от которых напрямую зависит функционирование печени, отечественными патоморфологами были описаны как зернистая, жировая дистрофия, отложение амилоидных масс, реже — аннулярный цирроз и некроз гепатоцитов [21].
Аналогичные изменения обнаружены в печеночной ткани при РА и другими исследователями [1,24]. Более того, в работе В.В.Василенкайтис ]4], продемонстрирована корреляция между структурно-функциональными печеночными нарушениями и активностью ревматоидного процесса.
В настоящее время общепризнанными являются два типа функционально- морфологических изменений печени при РА:
1. Отложение амилоидных масс по ходу внутридоль-ковых капилляров между звездчатыми эндотелиоцитами, в ретикулярной строме долек, стенках сосудов, протоков, межуточной ткани портальных трактов с атрофией гепатоцитов.
2. Воспалительные и склеротические изменения портальных трактов и стромы как морфологическое выражение иммунных нарушений [8, 17].
Нельзя также исключить влияние на печень лекарственных препаратов (в первую очередь, цитотоксических), используемых в терапии РА. Еще в 60-е годы высказывалось предположение о том, что при длительном применении антиревматических средств происходит ослабление окислительно-энергетических процессов, обусловливающее пониженное потребление тканями, в частности клетками печени кислорода [9].
По результатам анализа, проведенного в Институте ревматологии РАМН в течение 1999 г., у стационарных больных ревматическими заболеваниями в 6% случаев отмечалось повышение аминотрансфераз [5].
Адрес: 115522 Москва, Каширское шоссе, 34А Институт ревматологии РАМН
Нестероидные противовоспалительные препараты (НПВП), и модифицирующие болезнь (базисные) препараты широко применяются в ревматологии. НПВП — индуцированные гастропатии являются частым осложнением противовоспалительной терапии. Поражение печени, возникающее на фоне приема НПВП, также заслуживает внимания [12].
По данным одних авторов каких-либо клинических признаков НПВП-индуцированной гепатопатии не выявляется [44]. В то же время в литературе описано развитие «салицилового» гепатита, сопровождавшегося повышением уровня аминотрансфераз и подтвержденного исследованием биоптата печени [58].
По данным ряда авторов [29, 66], у больных РА на фоне приема НПВП может повышаться уровень аспартатами-нотрансферазы [АсАт], что, однако, редко служит поводом для отмены препарата. Описаны случаи развития внутрипе-ченочного холестаза на фоне приема пироксикама, подтвержденного компьютерной томографией и исследованием биоптата печени [39]. Отмечена гепатоксичность дикло-фенака у 7 больных РА (у 1 из них с летальным исходом) [38]. В сравнительном исследовании целекоксиба (специфический ингибитора ЦОГ-2) по сравнению с другими НПВП была показана более низкая его гепатоксичность [47].
К медленно действующим, болезнь модифицирующим средствам относят аминохинолиновые препараты, сульфа-салазин, соли золота, О-пеницилламин. При назначении О-пеницилламина отмечено развитие холестатической желтухи [20]. Изменение функции печени, в том числе повышение уровня аминотрансфераз, как побочный эффект сульфасалазина (СЗ), отмечен у 4,7% больных РА [61, 27, 32]. Описан также летальный исход, обусловленный массивным некрозом печени у больного с синдромом Шегре-на, принимавшего СЗ [48].
У больных РА с хроническим вирусным гепатитом повышение уровня аминотрансфераз выявлено в 53% случаев при применении плаквенила, в 55,6% — СЗ и не наблюдалось при использовании препаратов золота для внутримышечного введения и метотрексата (МТ) [50]. У одного пациента на фоне приема азатиоприна авторы выя вши активацию хронического вирусного гепатита В. Прием базисных средств больными РА с хроническим вирусным гепатитом чаше сопровождался проявлением гепатотоксичнос-ти препаратов по сравнению с группой больных РА без гепатита [50].
Цитотоксические иммунодепрессанты — МТ, циклофос-фамид (ЦФ), азатиоприн, циклоспорин А и их комбинации — все шире внедряются в практику ревматологов. Сообщают, что комбинация плаквенила и МТ приводит к уменьшению гепатоксичности последнего [41].
Но если в 60-е годы препараты, с возможным гепато-тропным действием (О-пеницилламин, цитотоксики) применяли сравнительно редко, в основном при рефрактерном РА, то в настоящее время тактика лечения изменилась и базисные препараты начинают включать в комплексное лечение на ранних стадиях РА. В первую очередь это касается «золотого стандарта» — МТ, при приеме которого отмечается умеренное повышение уровня аминотрансфераз, особенно аспарагиновой [20]. Дозозависимое транзиторное повышение уровня аминотрансфераз — нередкий побочный эффект МТ, проявляющийся через 4-5 дней от начала лечения и сохраняющийся в течение 1-2 недель после отме-
ны. Дву- или трехкратное повышение уровня аминотранс-фераз не является основанием для отмены МТ, а более существенное увеличение уровня ферментов свидетельствует
0 необходимости снижения дозы или прерывания лечения [15, 45, 63].
Ретроспективное изучение 188 аутопсийных случаев РА с 1958 по 1985 гг, т. е. до широкого использования МТ, выявило выраженное фиброзное поражение печени (3-4 балла) лишь в 2 случаях [62]. Другие авторы в биоптатах печени больных, длительно принимавших МТ. также обнаруживали умеренно выраженные гистологические изменения — жировую дегенерацию, перипортальную лимфоцитарную инфильтрацию и фиброз [67, 68, 69].
Факторами риска развития побочных эффектов со стороны печени при приеме МТ являются алкоголизм, пожилой возраст, ожирение, сахарный диабет, нарушение почечной функции, контакт с гепатотоксичными веществами [20].
Мнения, касающиеся опасности развития фиброза и цирроза печени на фоне лечения МТ, противоречивы. Полагают, что поражение печени чаще наблюдается при лечении МТ больных псориазом, чем РА [31]. Фиброз печени, по данным ряда исследователей обнаруживается почти у трети больных, получающих МТ более 2 лет, но цирроз развивается редко [25, 36, 60, 63].
Высокая инфицированность населения планеты вирусом гепатита В (около 2-х млрд. человек) и гепатитом С (около 500 млн. человек) делает значительным риск развития прогрессирующих хронических заболеваний печени, которые могут протекать как самостоятельное заболевание или сочетается с другими конкурентными болезнями [13].
К настоящему времени известны следующие вирусы гепатита: А (НАУ), В (НВУ ), С ( НСУ ), Ъ ( НОУ ), Е (НЕУ), Я ( НРУ ), в ( НСУ ), а также недавно открытые
1 ГУ, БЕЫ-У. Способность к хронизации в виде персисти-рования или латентно существующей (в течение длительного периода — до 20 лет), доказана для вирусов гепатита В, С, О. Большинство инфицированных считают себя здоровыми, оставаясь потенциальными источниками инфекции [2, 7, 18,19].
Исследования последнего десятилетия с использованием иммунологических, молекулярно-биологических (ПЦР, молекулярная гибридизация), а также морфологических методов, значительно расширили представление о патологии, обусловленной вирусами гепатита. До начала 90-х годов большинство вирусологов считало, что вирус гепатита В обладает строгой гепатотропностью. Однако, выявление антигенов не только в печени, но и в других органах (почки, селезенка, мышцы, лимфоузлы), заставило усомниться в этом. В 1989 году аналогичные данные были получены российскими молекулярными биологами и подтверждены на обширном клиническом материале [2]. Это позволило рассматривать вирусный гепатит не как болезнь печени, а как системный (генерализованный) процесс [2,7]. Особое внимание привлекли к себе доказательства репликации НСУ и НВУ в моноцитах и макрофагах [2], что может служить причиной «ускользания» вирусов гепатита В и С от иммунного надзора. Перенесенная НСУ инфекция не индуцирует прочной иммунной защиты, причем допускается возможность повторного заражения не только другими генотипами, но и гомологичными штаммами вируса [Ю].
В связи с тем, что одним из наиболее частых проявлений хронического вирусного гепатита С, особенно у больных криоглобулинемией, является суставная патология по типу моно- или олигоартрита (чаще — крупных и средних суставов), с интермиттирующим течением, но без деструкции суставных поверхностей, встает вопрос о взаимотно-шении хронического вирусного гепатита и РА.
Впервые актуальность изучения ревматологических аспектов хронического гепатита была сформулирована Е.М. Тареевым в 1979 г. [22]. Одно из первых описаний развития РА с типичной рентген’- ’-‘гичеокой картиной, гистоло-
гическими изменениями синовии и наличием РФ при остром гепатите принадлежит Е. L.Morris и M.V Stevens [51]. Позже подобные наблюдения были сделаны отечественными учеными (Е. М. Тареев, 3. Г. Апросина, Т. Н. Лопатки-на). Поводом для новой волны интереса к проблеме взаимосвязи РА и гепатита послужило описание клинических случаев дебюта РА после вакцинации против гепатита В у лиц с определенной генетической предрасположенностью (носители HLA-DR4 антигена), что позволило рассматривать вирус гепатита в качестве триггера в развитии РА [26, 50].
В этиологии РА в последние годы активно обсуждается роль хронической вирусной инфекции. Работы такого плана направлены на выделение экзогенного агента, способного вызвать иммунное воспаление в синовиальной ткани с его последующим самоподдержанием. Но хотя гипотеза, согласно которой в этиологии РА определенную роль играет вирус, широко обсуждается в литературе с начала 70-х годов, обнаружить латентные вирусы в клетках ревматоидной синовиальной ткани методами культивирования, кокультивирования и слияния клеток длительное время не удавалось. В пользу этой теории свидетельствовали лишь результаты электронно-микроскопических исследований ревматоидной синовиальной ткани, выявившие структуры, напоминающие вирусный материал или продукты взаимодействия вируса с клетками хозяина (35, 43, 53, 54]. Спектр вирусов как возможных триггеров РА весьма широк [6, 26,
28, 30, 33-35, 37, 40, 42, 43, 49, 52-57,59, 65]. Складывается впечатление, что для РА не существует единого этиологического агента.
Что касается вирусов гепатита, то, вероятнее всего, они повреждают макрофагальную систему печени, что приводит к снижению клиренса антигенов и иммуноглобулинов. Хроническая антигенная стимуляция сопровождается поли-и моноклональной пролиферацией В-лимфоцитов, повышенной продукцией иммуноглобулинов и образованием иммунных комплексов, в том числе смешанных криоглобулинов (КГ), накапливающихся в циркуляции [11]. По мнению некоторых авторов КГ могут проявлять РФ-активность и появляться на втором этапе регуляторного ответа как реакция на инфицирование или воспалительный процесс, протекающий в организме [11]. В последнее время все большим количеством исследований подтверждается тесная связь между НСУ инфекцией и «эссенциальной» криоглобулинемией. HCV-инфекция характеризуется уникальным иммунологическим феноменом — ни при какой другой инфекции не отмечается столь частой продукции РФ и столь высокой его специфичности. Вырабатывается не только поликлональный, преимущесвенно Ig М РФ, представляющий основу криоглобулинемии 3 типа, но особый клон В-лим-фоцитов, продуцирующих высокоспецифичный lg Mk [11].
Известно, что депозиция иммунных комплексов в стенках сосудов или in situ при активации системы комплемента приводят к развитию васкулита [14] и таким клиническим проявлениям, как кожный васкулит, пурпура, гломерулонефрит, нейропатия, феномен Рейно. Установлено, что частота обнаружения антител к НСУ у больных со смешанной криоглобулинемией достигает 70 %, НСУ РНК в сыворотках крови выявляется в 71-86%, а в криопрецитатах в 93 % случаев [11].
Клинические данные, а также высокий процент изменений функциональных проб печени у больных РА, при отсутствии в анамнезе печеночной патологии, могут свидетельствовать в пользу наличия у части пациентов хронической гепатотропной вирусной инфекции.
Скрининговый анализ 373 историй болезни пациентов с РА, наблюдавшихся в Институте ревматологии в 1999 г., выявил повышение АлАг у 29, АсАт у 23, щелочной фосфа-тазы у 15, ГГТП у 14 пациентов. Причем с приемом анти-ревматических препаратов эти изменения можно было связать лишь у 8 больных (5 — с МТ и 3 — с СЗ).
Уточнение характера поражения печени при РА имеет не только теоретическое, но и практическое значение, т. к. при патологии печени (в том числе хронических вирусных
гепатитах), чаще наблюдается затяжное течение и прогрессирование ревматических заболеваний.
Изучение роли вирусной инфекции и криоглобулине-мии в патогенезе РА диктует необходимость дальнейших исследований в этом направлении с использованием совре-
1. Абрикосов А. И., Струков А. И. Патологическая анатомия. Часть 1. Общепатологические процессы. М., Мед-гиз, 1953, 107-133.
2. Апросина 3. Г. Последние достижения в изучении вирусных гепатитов: от молекулярной биологии к лечению вирусного гепатита В. Русс. мед. журн. 1996, 4, 3, 174 — 179.
3. Балабанова Р. М. Ревматоидный артрит. В кн. Ревматические болезни, 1997, 257-295.
4. Василенкайтис В. В. Изучение гепатотоксичности некоторых иммунодепрессантов при РА и экспериментальном ревматоидно-артритогенном процессе. Соврем. вопр. ревматол. Вильнюс, 1972, 136-138.
5. Дыдыкина И. С., Муравьев Ю. В., Мамистова А. И., Новоселова Т. М. Характер регистрируемых побочных действий, возникших у больных в период лечения в клинике Института ревматологии РАМН. Науч.-прак-тич.ревматол., 2000,4, 46.
6. Егорова О. Н., Балабанова Р. М., Чувиров Г. Н. Значение выявляемых при ревматических заболеваниях антител к вирусам семейства Негреву^ае. Тер. архив, 1998, 5, 41-45.
7. Игнатова Т. М. Внепеченочные проявления хронической инфекции, обусловленной вирусом гепатита С. Практик, врач, 2000,34, 1, 22-24
8. Копьева Т.Н. Патология ревматоидного артрита. Под ред. А. И. Струкова. М., Медицина, 1980, 196-205.
9. Кошуг Р. Ревматоидный артрит и поражение печени (обзор литературы). Винница, 1979, 98-101.
10. Майер К. П. Гепатит и последствия гепатита. М., ГЭ-ОТАР — МЕД,2001,123.
11. Малышко Е.Ю., Крель П.Е. Смешанная криоглобули-немия, ассоциированная с вирусом гепатита С. Практик. врач ,2000,34, 1, 24 -25.
12. Муравьев Ю. В. Безопасна ли терапия антиревматиче-скими средствами? В кн. Избранные лекции по клинической ревматологии. Под ред. В. А. Насоновой, Н. В. Бунчука, М., Медицина, 2001, 225-232.
13. Мухин Н.А. Некоторые современные оценки тенденции развития гепатологии. Практик.врач, 2000, 17,1314.
14. Насонов Е. Л., Баранов А. А., 111 ил к и на Н.П. Васкули-ты и васкулопатии. Ярославль, 1999, 515-520.
15. Насонов Е. Л., Соловьев С. К. Применение метотрексата в ревматологии, М., 2000, 25- 26.
16. Никитин И. Г., Сторожаков Г. И. Хронический гепатит С: актуальные вопросы диагностики и лечения. Клин, перспект.гастроэнтерол., гепатол.,2001,3,7-11.
17. Раденска-Лоповок С.Г. Патоморфология ревматоидного артрита. В кн. Ревматические болезни, 1997, 261266. ‘
18. Серов В. В. Морфологическое исследование в диагностике и лечении острых и хронических заболеваний печени. Русс.мед. журн.,1996, том 4 ,3, 173 — 174.
19. Серов В.В. Современная классификация хронических гепатитов. Русс.мед. журн., 1996,том 4 ,3 ,179 — 183.
20. Сигидин Я. А., Лукина Г.В. Базисная (патогенетическая) терапия ревматоидного артрита. М., 2000, 36 — 59.
21. Струков А.И., Бегларян А.Г. Патологическая анатомия и патогенез коллагеновых болезней. М., 1963, 200-205.
22. Тареев Е. М., Апросина 3. Г., Лопаткина Т. Н., Копьева Т, Н., Попова И. В. Острый сывороточный гепатит как дебют ревматоидного артрита. Тер. архив, 1979, 51,10, 4-9.
23. Чичасова Н. В. Ревматоидный артрит: клинико-имму-
менных методов диагностики, включая иммунологические и морфологические. Решение проблемы позволит вскрыть механизм развития криоглобулинемии , а также уточнить тактику лечебных мероприятий при РА с сопутствующим инфицированием вирусами гепатита В и С.
нологические и клинико-морфологические сопоставления, прогноз. Доктор, дисс. М., 2000, 61 — 102.
24. Шуцяну Ш., Ионеску-Блажа В. Клиника и лечение ревматических заболеваний. Бухарест, Мед. изд-во, 1983,150-152.
25. Clegg D. О., Furst D. Е., Tolman К. G. et al. Acute reversible hepatic failure associated with methotrexate treatment of RA. J. Rheumatol., 1989,16,1123-1126.
26. Congia М., Clemente M.G., Dessi C. HLA class II genes in chronic hepatitis С virus-infection and associated immunological disorders. Hepatol., 1996, 24,6,1338-1341.
27. Donovan S., Hawley S., MacCarthy J. et al. Tolerability of enteric-coated suphasalazine in rheumatoid arthrirtis: results of a со- operating clinics study. Br. J. Rheumatol., 1990, 29,3, 201-204.
28. Eguchi K.Origuchi T.,Takashima H. et al. High seropreva-lence of anti-HTLV-I antibody in rheumatoid arthritis. Arthr. Rheum., 1996, 39,3, 463-466.
29. Freeland G. R., Northington R. S., Hedrich D. A. et al. Hepatic safety of two analgetics used over the counter: ibuprofen and aspirin. Clin, Pharmacol. Ther., 1988, 43,5,473-479.
30. Frenkel L.M., Nielsen K., Garakian A.A search for persistent rubeolla virus infection in person with chronic symptoms after rubeolla and rubeolla immunisation and in patient with juvenile rheumatoid arthritis. Clin. Infect. Dis., 1996,22,2,287-294.
31. Gilbert S. C., Klintman G., Menter A. et al. Methotrexate induced cirrhosis requiring liver transplantation in three patients with psoriasis. Arch. Int. Med., 1990,150,889- 891.
32. Gran J. Т., Myklebust G. Toxiticy of suphasalazine in rheumatoid arthrirtis. Possible protective effect of rheumatoid factors and corticosteroids Scand. J. Rheumatol., 1993,22,5,229-232.
33. Gran J.T., Jonsen V., Myklebust G. The variable clinical picture of arthritis induced by human parvovirus В19. Report of seven adult cases and review of literature. Scand. J. Rehumatol., 1995, 24,3, 174-179.
34. Guorin B., Numoric P., Jean-Baptiste G. et al. Polyarthritis in HTLV-I infected patients. A review of 17 cases. Rev. Rehum. Engl. Ed., 1995, 62,1, 21-28.
35. Hamerman D. Gresser I., Smith C. Isolation of cito-megalovirus from synovial cells of a patient with rheumatoid arthritis. J. Rheum., 1982,9,5, 658-664.
36. Hassan W. Methotrexate and liver toxicity: role of surveillance liver biopsy. Ann. Rheum. Dis. 1996,55, 273-275.
37. Hasunuma T. Pathomechanism of HTLV-I associated arthropathy and the role of tax gene. Nippon Rinsho, 1997,55,6.1482-1485.
38. Helfgott SM, Sandberg-Cook J, Zakim D. et al. Diclofenac-associated hepatotoxicity. JAMA. 1990, 28,264,20,2677-2678.
39. Hepps KS, Maliha GM, Estrada R. et al. Severe cholestatic jaundice associated with piroxicam. Gastroenterology., 1992,103,1,354-355.
40. Kahn M.F. Etiopatogenie de la polyarthrite rhumatoide. Ann. Med. Intern. 1981, 132,1, 3-5.
41. Khraishi MM, Singh G. The role of anti-malarials in rheumatoid arthritis-the American experience. Lupus., 1996,5,1,41-44.
42. Kingsley G., Panay G.S. Joint destruction in rheumatoid arthritis: biological bases. Clinical Exp. Rheum., 1997,15, suppl.17,3-4.
43. Koide J.,Takada K., Sugiura M. et al. Spontaneous establishment of an Epstein-Barr virus-infected fibroblast line
from the synovial tissue of a rheumatoid arthritis patient. Virol., 1997, 71,3,2478-2481.
44. Kraag G. R. Rare toxicity with nonsteroidal antiinflammatory drugs. J. Rheumatol., 1985, 12,1,1-3.
45. Kremer J.M., Furst D. E, Weinblatt M. E., Significant changes in serum AST across hepatic histological biopsy grades: an analysis of 3 prospective cohort on methotrexate therapy for rheumatoid arthritis. J.Rheumatol., 1996,23, 459-461.
46. Lomen P.,Turner L.F., Lambom K.R. Safety of ibuprofen in the treatment of ankylosing spondiylitis, osteoarthritis and rheumatoid arthritis. A summary of liver and kidney assay data. Am. J. Med., 1986,24, 80, 3A,23-30.
47. Maddrey W.C., Maurath C.J., Verburg K.M. et al. The hepatic safety and tolerability of the novel cyclooxygenase-
2 inhibitor celecoxib. Am. J. Ther., 2000,7,3,151-152.
48. Marinos G., Riley J., Painter D.M. et al. Sulfasalazine-induced fulminant hepatic failure. J. Clin. Gastroenterol., 1992,14,2,132-135.
49. McMurray R.W., Elboume K. Hepatitis C virus infection and autoimmunity. Semin.Arthr. Rheum., 1997, 26,4, 689701.
50. Mok MY, Ng WL, Yuen MF et al. Safety of disease modifying anti-rheumatic agents in rheumatoid arthritis. Patients with chronic viral hepatitis. Clin. Exp. Rheumatol., 2000,18,3,363-368.
51. Morris E. L., Stevens M. B. Rheumatoid arthritis — a sequel to HBsAg hepatitis. Am. J. Med., 1979,64,5, 859-862.
52. Motokawa S., Hasunuma T., Tajima K. et al. High prevalence of arthropathy in HTLV-I carries on Japanese island Ann. Rheum. Dis., 1996, 55,3, 193-195.
53. Murayama T., Jisaki F., Ayata M. et al. Citomegalovirus genomes demonstrated by polymerase chain reaction in synovial fluid from rheumatoid arthritis patients. Clin. Exp. Rheum., 1992, 10,161-164.
54. Musiani M., Zerbini M., Ferri S. et al. Comparison of the immune response to Epstein-Barr virus and cytomegalovirus in sera and synovial fluids of patients with rheumatoid arthritis. Ann. Rheum. Dis., 1987, 46, 837-842.
55. Nelson P.N. Retroviruses in rheumatic diseases. Ann. Rheum. Dis., 1995, 54, 441-442.
56. Newkirk M.M., Duffy K., Paleckova A. et al. Herpes virus-
es in multicase families with rheumatoid arthritis. J. Rheum., 1995, 22,11, 2055-2061.
57. Nishioka K. HTLV-1 arthropathy and Sjegren syndrome. J.Acquir.lmm.Defic.Syndr.Hum. Retroviral., 1996, 13,1,57-62.
58. O’Gorman T., Koff R.S. Salicylate hepatitis. Gastroenterology., 1977,72,4, 1,726-728.
59. Permin H., Aldershvile J. Hepatitis B virus infection in patients with rheumatic diseases.Ann. Rheum. Dis., 1982,
60. Philips C. A., Cera P J., Mangan T F. et al. Clinical liver disease in patients with RA taking methotrexate. J.Rheum., 1992, 19,229 -233.
61. Pullar T., Hunter J. A., Capell H. A Sulphasalazine and hepatic transaminases.Ann. Rheum. Dis., 1987,46,5, 421.
62. Ruderman E. M.,Crawford J. M. Histologic liver abnor-malityes in an autopsy series of patients with rheumatoid arthritis. Br. J. Rheum., 1997, 36, 210-213.
63. Shergy W.J., Polisson R.P., Cadwell D.S. et al. Methotrexate associated hepatotoxicity; retrospective analysis of 210 patients with RA. Am. J. Med., 1988,85,771 -777.
64. Singh G., Ramey D.R., Morfeld D. et al. Comparative toxicity of non-steroidal anti-inflammatory agents. Pharmacol. Ther., 1994,62,1-2,175-191.
65. Soderlung M., von Essen R., Haapasaari J. Persistence of parvovirus B19 DNA in synovial membranes of young patients with and without chronic arthropathy. Lancet, 1997,12,349,9058, 1063-1065.
66. Turner R. Hepatic and renal tolerability of long- term naproxen treatment in patients with rheumatoid-arthritis.Semin. Arthr. Rheum., 1987,17,suppl 2,29-35.
67. White — O A Keefe Q. E„ Fye K . H„ Sack C. D. Liver biopsy and methotrexate use: See no evil? Am. J. Gastroenterol., 1991,70,711-716.
68. White — O A Keefe Q. E., Fye K. H., Sack C. D. Methotrexate and histologic abnormalities: a meta -analysis. Am. J. Med., 1991,90,711-716.
Источник статьи: http://cyberleninka.ru/article/n/patologiya-pecheni-pri-revmatoidnom-artrite