Ингибиторы янус-киназ: перспективы применения при ревматоидном и псориатическом артрите и других ревматических заболеваниях
Ингибиторы янус-киназы подавляют внутри-клеточную сигнальную систему JAK/STAT, которая опосредует действие многочисленных цитокинов и факторов роста, играющих ключевую роль в патогенезе ревматических заболеваний. В отличие от генно-инженерных биологических препаратов (ГИБП), они предназначены для приема внутрь и не вызывают образование нейтрализующих антител. В ревматологии ингибиторы янус-киназ применяют в комбинации со стандартными базисными противовоспалительными препаратами (БПВП) у больных РА, не отвечающих на лечение БПВП или ГИБП, однако возможна и монотерапия тофацитинибом или барицитинибом, если одновременное применение БПВП по каким-то причинам невозможно или нежелательно (плохая переносимость, противопоказания). В исследовании ORAL Shift монотерапия тофацитинибом, которую проводили после отмены метотрексата у пациентов с РА, достигших низкой активности заболевания на фоне приема двух препаратов, по эффективности не уступала комбинированной терапии тофацитинибом и метотрексатом. В плацебо-контролируемых исследованиях установлена эффективность тофацитиниба в лечении псориатического артрита и псориаза, а также воспалительных заболеваний кишечника. Кроме того, эффективность и безопасность ингибиторов янус-киназ изучаются у больных анкилозирующим спондилитом и другими аутоиммунными заболеваниями.
Генно-инженерные препараты (ГИБП) в настоящее время применяют для лечения ревматоидного артрита (РА) и других заболеваний преимущественно в случае неэффективности или плохой переносимости стандартных базисных противовоспалительных препаратов (БПВП). ГИБП представляют собой моноклональные антитела, растворимые рецепторы или гибридные молекулы, которые блокируют функцию различных цитокинов, таких как фактор некроза опухоли (ФНО)-α, интерлейкин (ИЛ)-1b, ИЛ-6, ИЛ-17, ИЛ-23, или Т- и В-клеток, играющих ключевую роль в патогенезе ревматических заболеваний. В последние годы большой интерес у исследователей и разработчиков лекарственных средств вызывает изучение внутриклеточных сигнальных систем, опосредующих действие цитокинов и факторов роста, которое привело к появлению нового класса лекарственных препаратов, получивших название таргетных БПВП. Пока к этой группе относят только ингибиторы янус-киназ, оказывающие действие на внутриклеточную систему JAK/STAT, которая включает в себя янус-киназы (JAK1, JAK2, JAK3 и тирозинкиназу 2) и белок-трансдуктор и активатор транскрипции (STAT – signal transducer and activator of transcription) 2. При взаимодействии цитокина с соответствующим рецептором JAK фосфорилируют белки STAT, которые индуцируют транскрипцию генов, опосредующих действие цитокинов.
В Российской Федерации зарегистрированы два ингибитора янус-киназ – тофацитиниб и барицитиниб, однако в клинических исследованиях изучается еще около десятка подобных препаратов [4]. Все ингибиторы янус-киназ – это низкомолекулярные синтетические препараты. В отличие от ГИБП, они предназначены для приема внутрь и не обладают иммуногенностью, т.е. не вызывают образование антител, которые могут нейтрализовать активность белковых молекул и снизить эффективность лечения. В ревматологии ингибиторы янус-киназ применяют для лечения РА и псориатического артрита (ПсА), однако в ближайшем будущем можно ожидать расширения показаний к назначению этих препаратов.
Тактика применения ингибиторов янус-киназ для лечения ревматодного артрита
В рекомендациях Европейской антиревматической лиги (EULAR) 2016 г. лечение РА было предложено начинать с монотерапии стандартными БПВП, прежде всего метотрексатом, дозу которого следует быстро увеличить до 25-30 мг/нед в случае хорошей переносимости [5]. Если в течение 6 мес не удается добиться низкой активности или ремиссии РА, то при наличии неблагоприятных прогностических факторов (сохраняющаяся высокая активность заболевания, аутоантитела, ранние эрозии, отсутствие ответа на два БПВП) к терапии целесообразно присоединить ГИБП или ингибитор янус-киназ. При выборе между последними предпочтение было отдано ГИБП, учитывая больший опыт их применения в клинической практике.
Недавно были опубликованы обновленные рекомендации EULAR по лечению РА [6]. В целом стратегия лечения этого заболевания не претерпела особых изменений, в частности препаратом первой линии по-прежнему остается метотрексат. Тем не менее, изменения коснулись выбора препаратов второй линии. В новой версии рекомендаций повышена роль ингибиторов янус-киназ, т.е. сегодня при выборе тактики дальнейшей терапии у пациентов, не ответивших на метотрексат или другие стандартные БПВП, нет оснований отдавать предпочтение именно ГИБП и рассматривать таргетные БПВП как препараты “резерва». Основанием для пересмотра рекомендаций EULAR послужили результаты клинических исследований, подтвердивших высокую эффективность и благоприятный профиль безопасности ингибиторов янус-киназ в лечении РА, а также накопление опыта их применения в клинической практике. Так, к апрелю 2019 года в мире тофацитиниб получали более 200 000 больных РА.
Программа регистрационных исследований ингибиторов янус-киназ была сходной и предусматривала изучение различных схем их применения преимущественно у больных РА, у которых лечение стандартными БПВП и/или ГИБП не позволило достичь необходимого ответа. Эффективность и безопасность тофацитиниба в комбинации со стандартными БПВП сравнивали с плацебо и/или адалимумабом в 5 исследованиях, в том числе ORAL Scan, ORAL Standard, ORAL Sync, ORAL Step и ORAL Strategy [7]. Во всех этих исследованиях тофацитиниб оказывал быстрое действие (в течение 2-4 недель), а его присоединение к метотрексату или другим стандартным БПВП по сравнению с плацебо приводило к значительному увеличению частоты ответа на лечение, улучшению качества жизни и функциональной активности и задерживало прогрессирование рентгенологических изменений суставов. В рандомизированном исследовании ORAL Standard у 717 больных РА, у которых сохранялась умеренная или высокая активность заболевания на фоне терапии метотрексатом в стабильной дозе, частота ответа по критериям Американской коллегии ревматологов (АКР20) через 6 мес после присоединения тофацитиниба в дозах 5 или 10 мг два раза в день (51,5% и 52,6%, соответственно) почти в два раза превышала таковую в группе плацебо (28,3%, p
Монотерапия ингибиторами янус-киназ при РА
ГИБП и таргетные БПВП рекомендуется применять в сочетании с метотрексатом или другими стандартными БПВП. Однако результаты различных регистров, которые проводятся в Европе и США, свидетельствуют о том, что около трети больных РА получают ГИБП в виде монотерапии, что может быть связано с плохой переносимостью БПВП, наличием противопоказаний к их назначению или сопутствующих заболеваний [1416]. По данным регистра Swiss RA (SCQM-RA), в который были включены более 3000 пациентов с РА, факторами, ассоциировавшимися с назначением монотерапии ГИБП, были пожилой возраст, сопутствующие заболевания, длительность РА и более высокая его активность, низкий индекс массы тела, а также опыт применения ГИБП в анамнезе [14]. Сходные данные были получены и в регистре Британского общества ревматологов [17]. Создается впечатление, что врачи назначают монотерапию ГИБП больным РА, лечение которых представляет собой более сложную задачу.
Данные наблюдательных исследований, проводившихся в обычной клинической практике, свидетельствуют о том, что от 10 до 77% больных РА прекращают прием метотрексата из-за нежелательных эффектов [18]. Основным фактором риска развития нежелательных явлений при лечении метотрексатом является низкая скорость клубочковой фильтрации, которая приводит к снижению клиренса метотрексата и повышению его концентрации в сыворотке. Не все пациенты сообщают врачу о том, что они не принимают метотрексат в комбинации с ГИБП, например, из-за легких нежелательных явлений или нежелания отказываться от приема алкоголя. По данным исследования, проводившегося в Канаде на основании анализа аптечных баз данных, около трети больных РА не приобретали выписанные им БПВП, в том числе метотрексат, в течение 6 мес после назначения ГИБП [19]. С одной стороны, приведенные данные свидетельствуют о том, что в клинической практике ревматологам следует строже контролировать сделанные назначения, но с другой стороны, очевидно существование группы больных РА, у которых применение препаратов второй-третьей линии возможно только в виде монотерапии.
Как тофацитиниб, так и барицитиниб разрешено назначать в виде монотерапии. Эффективность монотерапии тофацитинибом изучалась в трех исследованиях, в том числе ORAL Strategy, ORAL Start и ORAL Solo. В двойное слепое, плацебо-контролируемое исследование ORAL Solo были включены 611 больных РА, у которых сохранялась активность заболевания несмотря на лечение стандартными БПВП или ГИБП [20]. Через 3 мес после начала монотерапии тофацитинибом в дозах 5 или 10 мг два раза в сутки частота ответа по критериям АКР20 (59,8% и 65,7%, соответственно) была достоверно выше, чем в контрольных группах больных, получавших плацебо (26,7%; p
Исследование ORAL-Shift
У части больных РА применение современных антиревматических препаратов в сочетании со стандартными БПВП позволяет достичь стойкой ремиссии, что позволяет обсуждать возможность уменьшения интенсивности иммуносупрессивной терапии. Очевидные достоинства такого подхода включают в себя снижение риска нежелательных явлений и затрат и улучшение приверженности к терапии [25]. Из экономических соображений эксперты EULAR в таких случаях рекомендуют отменять ГИБП и продолжать монотерапию стандартными БПВП [4]. Следует отметить, что полная отмена ГИБП более чем у половины пациентов приводит к развитию обострения РА 26, поэтому на первом этапе можно попытаться снизить дозу препарата или увеличить интервалы между его введениями. Факторы, позволяющие предсказать сохранение достигнутого ответа на лечение после прекращения введения ГИБП, включают в себя ранний РА, глубину и длительность ремиссии [28].
Высокая частота рецидивов РА после отмены ГИБП позволяет обсуждать целесообразность альтернативного подхода к ослаблению интенсивности иммуносупрессивной терапии путем отмены БПВП. Доводом в пользу подобной практики может служить и тот факт, что ГИБП или таргетные БПВП чаще всего назначают пациентам, у которых стандартные БПВП оказываются недостаточно эффективными. В рандомизированном исследовании TARA были сопоставлены результаты постепенной отмены (в течение 6 мес) стандартных БПВП или ингибиторов ФНО-α у 189 больных РА, у которых была достигнута ремиссия заболевания на фоне комбинированной терапии двумя препаратами [29]. Полной отмене БПВП предшествовало последовательное двукратное снижение дозы в два раза под контролем активности РА, в то время как ингибитор ФНО-α отменяли после увеличения интервала между введениями в два раза и последующего снижения дозы. Через 1 год кумулятивная частота рецидивов РА (33% и 43% после отмены БПВП и ингибиторов ФНО-α, соответ ственно) и значения счета DAS, HAQ-DI и EQ-5D достоверно не отличались между группами, хотя обращала на себя внимание тенденция к увеличению риска развития рецидива после отмены ГИБП по сравнению с БПВП. В отдельных исследованиях изучали результаты отмены стандартных БПВП у пациентов, получавших их в комбинации с ингибиторами ФНО-α или ИЛ-6. Например, в исследованиях COMP-ACT и JUST-ACT монотерапия тоцилизумабом после отмены метотрексата по эффективности не уступала продолжающейся комбинированной терапии тоцилизумабом и метотрексатом у пациентов с РА, достигших низкой активности заболевания [30,31].
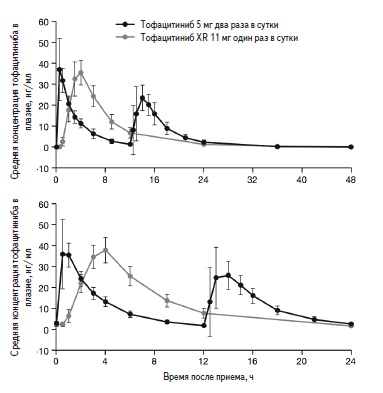
Недавно были опубликованы результаты исследования ORAL Shift, в котором изучалась возможность отмены метотрексата у больных РА, достигших низкой активности заболевания на фоне комбинированной терапии тофацитинибом и метотрексатом [32]. В этом исследования применялась новая форма тофацитиниба, которую можно назначать один раз в день. В фармакокинетическом исследовании установлена биоэквивалентность тофацитиниба модифицированного высвобождения в дозе 11 мг один раз в день и стандартной формы тофацитиниба в дозе 5 мг два раза в день (рис. 1) [33]. В открытую 24-недельную фазу исследования были включены 694 больных РА, у которых сохранялась активность заболевания несмотря на лечение метотрексатом в дозе 15-25 мг/нед в течение по крайней мере 4 мес. Во время первой фазы все пациенты получали тофацитиниб модифицированного высвобождения в дозе 11 мг один раз в сутки и метотрексат. У 533 из 623 больных, продолжавших комбинированную терапию в течение 24 недель, была достигнута низкая активность РА, которую оценивали на основании счета CDAI (≤10). Во вторую 24-недельную двойную слепую фазу исследования были включены 533 больных с низкой активностью РА, которых рандомизировали на две группы: у 267 пациентов основной группы метотрексат был заменен на плацебо, т.е. они продолжили монотерапию тофацитинибом, в то время как у 266 больных группы сравнения во время второй фазы проводилась комбинированная терапия тофацитинибом и метотрексатом. Первичный анализ эффективности двух схем терапии предполагал сравнение изменений счета DAS28-4(СОЭ).
Две группы были сопоставимы по демографическим и клиническим показателям. Во время двойной слепой фазы активность РА в обеих группах оставалась низкой, а достоверной разницы изменения счета DAS28-4(СОЭ) между двумя группами выявлено не было. Это позволило сделать вывод о том, что монотерапия тофацитинибом после отмены метотрексата у больных РА, достигших низкой активности заболевания на фоне комбинированной терапии, по эффективности не уступала продолжению комбинированной терапии. В конце исследования частота ответа по критериям АКР20 и АКР70 была сходной в группах больных, получавших монотерапию тофацитинибом и комбинированную терапию, в то время как частота ответа по критериям АКР50 была ниже на фоне монотерапии (55% и 67%, соответственно). У большинства больных двух групп во время двойной слепой фазы не были зарегистрированы обострения РА (нарастание счета DAS28-4(СОЭ)≥1,2 по сравнению с таковым перед рандомизацией). Доля больных, у которых отмечались обострения РА, в двух группах была сопоставимой как через 36 недель (16% и 13%, соответственно), так и через 48 недель (14% и 9%).
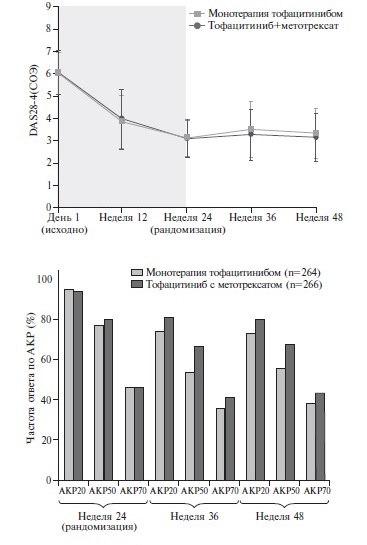
Таким образом, первичный и большинство вторичных показателей активности РА оставались стабиль ными после отмены метотрексата у больных, продолжавших монотерапию тофацитинибом, которая по эффективности не уступала комбинированной терапии тофацитинибом и метотрексатом. Переносимость двух схем была сопоставимой. Это не было неожиданным, так как больные, которые плохо переносили тофацитиниб или метотрексат, были исключены из исследования во время открытой фазы. Результаты исследования ORAL-Shift показали, что у больных РА, достигших низкой активности заболевания на фоне комбинированной терапии тофацитинибом и метотрексатом, отмена стандартного БПВП не приводит к ухудшению эффективности лечения. Следует обратить внимание на то, что более чем у 85% больных, получавших монотерапию ингибитором янус-киназ, не были зарегистрированы обострения РА, частота которых была сходной с таковой на фоне комбинированной терапии.
Эффективность тофацитиниба в лечении псориатического артрита
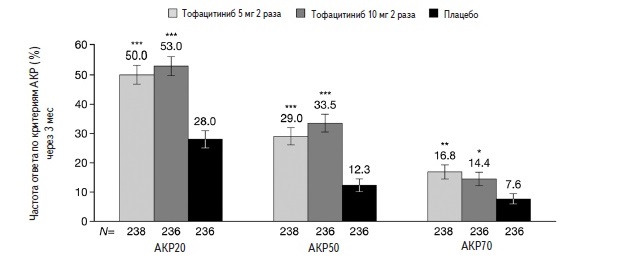
Тофацитиниб стал первым ингибитором янус-киназ, зарегистрированным для лечения бляшечного псориаза и ПсА. Эффективность и безопасность тофацитиниба в дозах 5 и 10 мг два раза в сутки в лечении ПсА изучались в двух плацебо-контролируемых исследованиях в целом у 710 больных, не ответивших на лечение стандартными БПВП (ORAL Broaden) или комбинированную терапию БПВП и ингибиторами ФНО-α (ORAL Beyond) 35. В обоих исследованиях ингибитор янус-киназ применяли в сочетании со стандартными БПВП, чаще всего метотрексатом. В исследовании ORAL Broaden была выделена также группа больных, которые получали адалимумаб. Через 3 мес частота ответа по критериям АКР20 в группах тофацитиниба (50,0-53,0%) достоверно превышала таковую в группе плацебо (28,0%) (рис. 3). Сходные результаты были получены при анализе ответа по критериям АКР50 и АКР70. Кроме того, лечение тофацитинибом привело к более значительному улучшению функциональной активности больных, которую оценивали на основании счета HAQ-DI, и снижению числа болезненных и опухших суставов. Преимущество тофацитиниба перед плацебо было отмечено и при оценке эффективности лечения псориаза (частота улучшения по критериям PASI75), энтезита и дактилита, а также спондилита (счет BASDAI). В исследовании ORAL Broaden тофацитиниб по эффективности существенно не отличался от адалимумаба.
Перспективы применения ингибиторов янус-киназ при анкилозирующем спондилите
Ингибиторы янус-киназ модулируют активность ИЛ17, ИЛ-21, ИЛ-23 и ФНО-α, которые играют ключевую роль в патогенезе анкилозирующего спондилита (АС), что открывает перспективы их применения при этом заболевании. Эффективность тофацитиниба в различных дозах (2, 5 и 10 мг два раза в сутки) в лечении АС изучалась в плацебо-контролируемом 16-недельном исследовании 2 фазы у 206 больных, не ответивших на нестероидные противовоспалительные препараты или плохо переносивших эти препараты [37]. По частоте ответа по критериям ASAS20 через 12 недель (первичный показатель эффективности) тофацитиниб в дозе 5 мг два раза в сутки достоверно превосходил плацебо (80,8% и 41,2%, соответственно, p
Заключение
Пероральные ингибиторы янус-киназ, которые представляют собой малые молекулы, не обладающие иммуногенностью, все чаще применяют как альтернативу ГИБП у больных РА, не отвечающих на лечение метотрексатом или другими БПВП. В клинических исследованиях эффективность ингибиторов янус-киназ установлена и у больных РА, у которых терапия ингибиторами ФНО-α не позволила достичь необходимого ответа. Как правило, ингибиторы янус-киназ целесообразно назначать в комбинации со стандартными БПВП, однако при необходимости, например, при плохой переносимости БПВП или при наличии противопоказаний к их применению, возможна и монотерапия тофацитинибом или барицитинибом. В исследовании ORAL Shift у больных РА, достигших низкой активности заболевания в результате терапии тофацитинибом с метотрексатом, отмена последнего не приводила к ухудшению результатов лечения, в частности повышению частоты обострений, по сравнению с продолжением комбинированной терапии. Тофацитиниб стал первым ингибитором янус-киназ, зарегистрированным для лечения ПсА, псориаза и язвенного колита. В настоящее время изучаются новые показания к применению препаратов этой группы, в частности в клиническом исследовании 2 фазы была показана эффективность тофацитиниба у больных АС, что обосновывает дальнейшей изучение его в клинических исследованиях 3 фазы.
Источник статьи: http://clinpharm-journal.ru/articles/2020-1/ingibitory-yanus-kinaz-perspektivy-primeneniya-pri-revmatoidnom-i-psoriaticheskom-artrite-i-drugih-revmaticheskih-zabolevaniyah/